AlphaFold: A inteligência artificial que decifrou o quebra-cabeça da vida
AIUma inteligência artificial do Google decifrou a linguagem da vida. O AlphaFold resolveu um problema de 50 anos e está abrindo as portas para uma nova era na medicina e na tecnologia. Saiba como essa revolução vai mudar o seu mundo neste artigo.

Olha eu de novo. Esse mês estou escrevendo como nunca! Hoje, vamos falar sobre mais uma das maiores revoluções científicas do nosso século, algo que soa como ficção científica, mas é a mais pura e impactante realidade. Peguem o café, ajeitem-se na cadeira, porque vamos mergulhar no universo do AlphaFold, a inteligência artificial (IA) do Google que está mudando tudo o que sabemos sobre a biologia.
Sabe quando você monta um quebra-cabeça de milhares de peças? Você tem todas as pecinhas ali, espalhadas, mas o verdadeiro desafio é descobrir como cada uma se encaixa para formar a imagem final. Agora, imagine que esse quebra-cabeça é a própria vida, e as peças são os blocos de construção de todos os seres vivos. Por 50 anos, os cientistas mais brilhantes do mundo tentaram resolver esse enigma, um dos mais difíceis e importantes da biologia. E então, em 2020, uma IA chegou e, em questão de dias, apresentou a solução com uma precisão que deixou o mundo boquiaberto.
Essa é a história do AlphaFold. Mas este post não é só para contar essa história. É para te mostrar por que essa conquista é tão monumental e como ela vai impactar sua vida, da medicina que você tomará no futuro aos alimentos que comerá e até mesmo a forma como combatemos as mudanças climáticas. Dividi em 5 partes.
Parte 1: O que são proteínas e por que a sua forma é TUDO?
Antes de falarmos do super-herói (o AlphaFold), precisamos entender o universo em que ele atua. E esse universo é o das proteínas.
Esqueça a imagem do whey protein que você toma na academia por um segundo. As proteínas são muito, mas muito mais do que isso. Elas são as verdadeiras operárias, engenheiras, mensageiras e soldadas do seu corpo. Tudo o que acontece dentro de você, desde a digestão do seu almoço até a leitura deste texto, é orquestrado por elas.
Pense no seu corpo como uma cidade imensa e movimentada. As proteínas seriam:
- Os operários: construindo novas células e reparando tecidos (como o colágeno).
- Os caminhões de entrega: transportando substâncias vitais, como o oxigênio que a hemoglobina leva para todo o corpo.
- As telefonistas: transmitindo sinais entre as células (hormônios como a insulina são proteínas).
- As seguranças: defendendo seu corpo contra invasores (os anticorpos são proteínas).
- As catalisadoras: acelerando reações químicas essenciais para a vida (as enzimas são proteínas).
Basicamente, elas fazem... tudo.
Mas aqui está o pulo do gato, a informação mais importante desta parte: a função de uma proteína é definida pela sua forma 3D.
Toda proteína começa como uma longa corrente, um colar de contas feito de pequenas moléculas chamadas aminoácidos. Existem 20 tipos principais de aminoácidos, e a sequência em que eles são enfileirados é ditada pelo nosso DNA. É como uma receita.
O problema é que essa corrente não fica esticada. Assim que é criada, ela se dobra e se enovela sobre si mesma de uma forma incrivelmente complexa e específica, formando uma estrutura tridimensional única. É um verdadeiro origami molecular.
E é essa forma final, essa escultura 3D, que determina o que a proteína faz. Pense numa chave e numa fechadura. A forma da chave (a proteína) precisa ser perfeita para encaixar na fechadura (outra molécula) e realizar sua tarefa. Se a forma estiver errada, a chave não funciona. Uma enzima que deveria quebrar açúcar não vai funcionar se não tiver o "bolso" com o formato exato para a molécula de açúcar se encaixar. Um anticorpo não vai neutralizar um vírus se não tiver a "garra" com o formato preciso para se prender a ele.
Resumindo: Sequência de aminoácidos (1D) → Forma da Proteína (3D) → Função Biológica (A Mágica da Vida).
Saber a forma de uma proteína é saber o seu segredo. É entender como ela funciona, por que ela para de funcionar numa doença e como podemos interagir com ela para consertá-la. O problema? Descobrir essa forma era um pesadelo.
Parte 2: O desafio de 50 anos – o "Santo Graal" da biologia
Ok, então sabemos que a forma 3D é crucial. A pergunta óbvia é: por que não a descobrimos para todas as proteínas?
Aí entramos no que é conhecido como o "problema do enovelamento de proteínas" (protein folding problem), considerado por meio século um dos maiores e mais importantes desafios não resolvidos da ciência.
O problema é o seguinte: a partir da sequência de aminoácidos (que é fácil de obter com o sequenciamento de DNA), como prever a estrutura 3D final em que ela vai se dobrar?
Parece simples, mas não é. Um proteinólogo chamado Cyrus Levinthal calculou que, para uma proteína de tamanho médio, o número de formas possíveis que ela poderia assumir é astronomicamente grande. Se ela tentasse cada uma delas para achar a correta, levaria mais tempo do que a idade do universo. No entanto, na natureza, uma proteína se enovela em sua forma correta em meros milissegundos. Esse é o Paradoxo de Levinthal. Claramente, a natureza não joga dados; ela segue um caminho, uma "receita de dobra" que os cientistas não conseguiam decifrar.
Por décadas, as únicas maneiras de descobrir a estrutura de uma proteína eram através de métodos experimentais caríssimos, demorados e terrivelmente difíceis, como a cristalografia de raios-X e a crio-microscopia eletrônica. Pense nesses métodos como tirar uma "foto" da proteína. Para isso, você precisa de equipamentos que custam milhões, anos de trabalho de um especialista e, muitas vezes, a proteína simplesmente não "colabora" – ela não cristaliza ou não fica quieta para a foto.
O resultado? Em 2020, tínhamos as sequências de centenas de milhões de proteínas, mas conhecíamos a estrutura experimental de menos de 0,1% delas. Era como ter um dicionário com milhões de palavras, mas sem saber o significado da vasta maioria. Estávamos voando às cegas.
Para estimular a pesquisa, foi criada uma competição bianual chamada CASP (Avaliação Crítica de Técnicas para Predição da Estrutura de Proteínas). Era a Copa do Mundo da área, onde grupos de pesquisa do mundo todo recebiam sequências de proteínas cujas estruturas haviam sido descobertas experimentalmente (mas ainda não publicadas) e tentavam prevê-las computacionalmente. Por anos, os resultados foram... medíocres.
Até que a DeepMind, uma empresa de IA do Google, entrou na arena.
Parte 3: Como o AlphaFold funciona?
A DeepMind já era famosa por criar IAs que venceram os melhores jogadores do mundo em xadrez e Go, jogos de estratégia complexa. Eles decidiram, então, mirar em um desafio do mundo real: o enovelamento de proteínas.
Em 2018, uma primeira versão do AlphaFold participou do CASP e venceu, com resultados bem melhores que os concorrentes. Foi impressionante, mas ainda não era a solução definitiva.
Dois anos depois, no CASP14 em 2020, eles apresentaram o AlphaFold 2. E o mundo da ciência mudou para sempre.
O AlphaFold 2 não foi apenas melhor. Ele foi revolucionário. Ele previu as estruturas das proteínas com uma precisão tão alta que era indistinguível dos resultados experimentais. Para muitos dos alvos, ele resolveu o problema. O desafio de 50 anos havia sido, em grande parte, superado.
Mas como ele faz isso? Sem entrar no detalhe técnico dos "transformers" e "redes de atenção" (que são os mecanismos de IA por trás dele), vamos usar uma analogia.
Imagine que a IA é um gênio que está aprendendo uma língua antiga e desconhecida (a linguagem das proteínas).
- Estudando a gramática evolutiva: Primeiro, o AlphaFold olha para a sequência de aminoácidos da proteína que quer decifrar. Então, ele vasculha um gigantesco banco de dados de proteínas conhecidas e procura por sequências parecidas em outras espécies. A lógica é que, se duas partes da "frase" (a sequência) foram conservadas juntas pela evolução ao longo de milhões de anos, mesmo em espécies diferentes, elas provavelmente são importantes e devem estar próximas na estrutura 3D final. É como perceber que, em várias línguas, as palavras "pão" e "manteiga" aparecem juntas com frequência, sugerindo uma relação.
- Construindo um mapa de relações: Com essas pistas, a IA começa a construir um "gráfico" de quais aminoácidos provavelmente estão perto uns dos outros no espaço. Ela não olha só para os vizinhos diretos na corrente; ela usa um mecanismo de "atenção" para avaliar a importância de cada aminoácido em relação a todos os outros, não importa quão distantes estejam na sequência inicial. É como ler uma frase inteira de uma vez para entender o contexto, em vez de ler palavra por palavra.
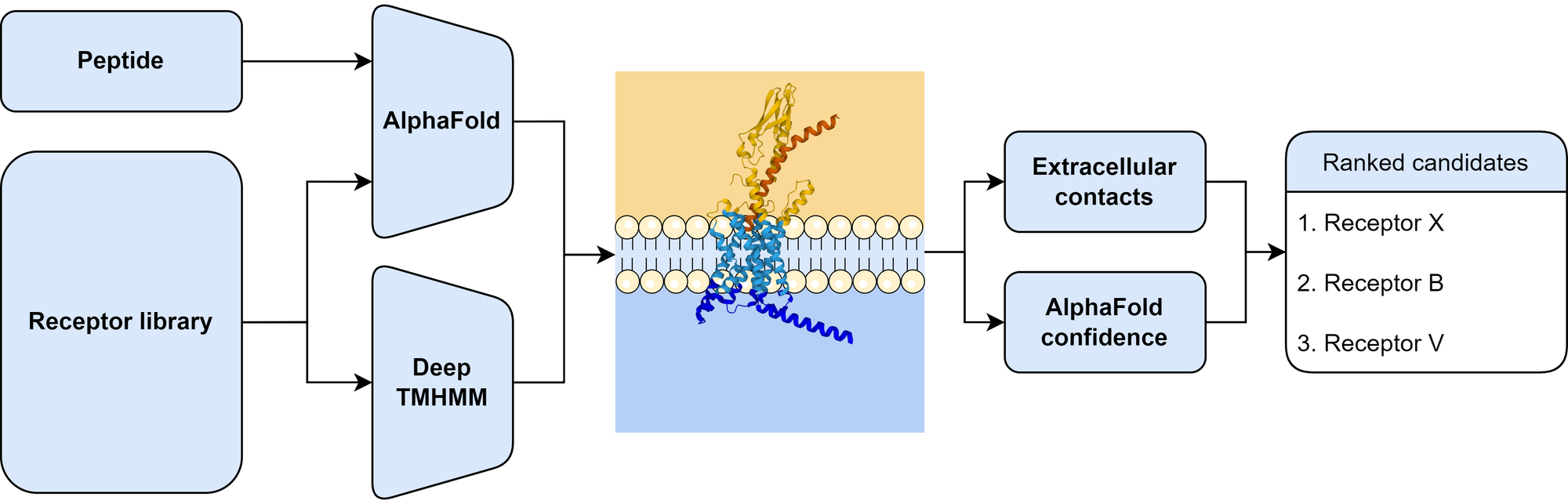
- Gerando e verificando a estrutura 3D: A partir desse mapa de relações, a IA propõe uma estrutura 3D. E aqui vem uma das partes mais geniais: o AlphaFold também foi treinado para prever a sua própria confiança em cada parte da previsão. Ele colore a estrutura 3D que gera. Partes em azul-escuro são previsões de altíssima confiança; partes em amarelo ou laranja são de baixa confiança. Isso é incrivelmente útil para os cientistas, pois diz a eles: "Confie nesta parte do meu trabalho, mas seja cético sobre esta outra parte aqui, ela provavelmente é mais flexível ou desordenada".
O golpe de mestre veio em seguida. Em vez de guardar essa tecnologia a sete chaves, a DeepMind, em parceria com o EMBL-EBI (Laboratório Europeu de Biologia Molecular), criou o AlphaFold Protein Structure Database e o tornou totalmente gratuito e acessível a todos. Eles não publicaram apenas as estruturas de todas as proteínas humanas. Eles publicaram as estruturas de praticamente todas as proteínas conhecidas pela ciência – mais de 200 milhões de estruturas.
Eles não deram aos cientistas a vara de pescar; eles entregaram todos os peixes do oceano, já limpos e prontos para cozinhar. Foi uma das maiores contribuições para o avanço da ciência da história.
Sua Alexa nunca será inteligente de verdade, e a ciência acaba de provar o porquê
Parte 4: O que o futuro nos reserva?
E agora, a parte que todos esperavam. Ok, resolvemos o quebra-cabeça. E daí? O que isso muda na prática? A resposta é: quase tudo. Estamos no começo de uma nova era, e estas são apenas algumas das portas que o AlphaFold está abrindo.
4.1 - Uma nova era para a medicina
Esta é talvez a área de impacto mais imediato e profundo.
- Desenvolvimento de remédios na velocidade da luz: Tradicionalmente, descobrir um novo remédio é um processo de tentativa e erro que custa bilhões de dólares e leva mais de uma década. Os cientistas testam milhares de moléculas para ver se alguma "gruda" na proteína-alvo de uma doença. Com o AlphaFold, podemos ver a forma exata da fechadura (a proteína da doença). Agora, em vez de testar chaves aleatórias, podemos desenhar computacionalmente a chave perfeita, uma molécula que se encaixe como uma luva para bloquear ou ativar aquela proteína. Isso vai acelerar drasticamente a descoberta de novos tratamentos para câncer, infecções bacterianas resistentes a antibióticos e doenças virais.
- Entendendo a raiz das doenças: Muitas doenças devastadoras, como alzheimer, parkinson e fibrose cística, são causadas por proteínas que se "dobram errado". Elas assumem uma forma tóxica que se acumula e danifica as células. Antes do AlphaFold, era muito difícil visualizar essa forma errada. Agora, podemos modelar como e por que isso acontece, abrindo caminhos para criar drogas que impeçam esse enovelamento defeituoso ou ajudem a "limpar" as proteínas tóxicas.
- Medicina personalizada de verdade: Todos nós temos pequenas variações em nosso DNA, o que significa que nossas proteínas podem ser ligeiramente diferentes. Uma mutação genética pode alterar um único aminoácido na corrente. Com o AlphaFold, podemos prever como essa pequena mudança afeta a forma 3D final da proteína. Isso pode explicar por que um remédio funciona para uma pessoa e não para outra, ou por que alguém tem uma predisposição a certa doença. O tratamento do futuro poderá ser desenhado com base na forma exata das suas proteínas.
- Vacinas mais rápidas e eficazes: Na pandemia de COVID-19, os cientistas correram para determinar a estrutura da proteína "Spike" do coronavírus, o alvo principal das vacinas. Isso levou meses com métodos tradicionais. Hoje, se um novo vírus surgir, o AlphaFold pode prever a estrutura de suas proteínas em questão de horas, permitindo que o desenvolvimento de vacinas comece quase que imediatamente.
4.2 - Revolucionando a indústria e o meio ambiente
O impacto vai muito além da saúde humana.
- Enzimas sob medida para um planeta mais limpo: Enzimas são proteínas que aceleram reações químicas. Elas são as ferramentas da natureza. Com o AlphaFold, entramos na era do design de enzimas.
- Comendo plástico: Cientistas já encontraram bactérias que conseguem "comer" plástico, mas suas enzimas são lentas. Agora, podemos visualizar essas enzimas, entender como funcionam e usar IA para modificá-las, criando "super-enzimas" capazes de degradar toneladas de lixo plástico de forma eficiente e barata, transformando poluição em matéria-prima.
- Biofuels de segunda geração: Podemos desenhar enzimas muito mais eficientes para quebrar celulose (de restos de plantas, por exemplo) e transformá-la em biocombustíveis, criando uma fonte de energia limpa e renovável que não compete com a produção de alimentos.
- Indústria química verde: Substituir processos químicos industriais poluentes e que consomem muita energia por reações catalisadas por enzimas que funcionam em temperatura ambiente e com água, tornando a indústria mais sustentável.
4.3 - Desvendando os mistérios fundamentais da biologia
O AlphaFold é como o Telescópio Espacial James Webb, mas para o universo interior das nossas células.
- Iluminando a "matéria escura" do genoma: Nós conhecíamos a "receita" (sequência) de milhões de proteínas, mas não tínhamos ideia do que a maioria delas fazia, porque não sabíamos sua forma. Com o banco de dados do AlphaFold, os cientistas podem agora pegar uma proteína de função desconhecida, olhar sua estrutura 3D e ter uma excelente pista sobre sua função. "Olha, essa proteína tem um formato parecido com uma tesoura, talvez ela corte alguma coisa!". Isso está acelerando a descoberta biológica a um ritmo sem precedentes.
- Mapeando as máquinas celulares: As proteínas raramente trabalham sozinhas. Elas se juntam para formar máquinas moleculares complexas. Um exemplo é o complexo do poro nuclear, o portão de segurança que controla tudo o que entra e sai do núcleo da célula. É uma megaestrutura feita de mais de 1000 proteínas. Por décadas, seu mapa era incompleto. Com a ajuda do AlphaFold, os cientistas conseguiram montar o quebra-cabeça e criar o modelo mais completo já feito dessa máquina crucial, um feito que a revista Science considerou um dos avanços do ano.
4.4 - Agricultura e segurança alimentar
- Culturas mais fortes: Podemos entender as proteínas que tornam as plantas resistentes a pragas, secas e doenças. Com esse conhecimento, podemos usar a engenharia genética de forma muito mais precisa para criar culturas que sobrevivam em climas mais hostis e exijam menos pesticidas.
- Reduzindo a necessidade de fertilizantes: Alguns dos maiores poluentes da agricultura são os fertilizantes nitrogenados. Existem bactérias que conseguem capturar nitrogênio do ar (um processo feito pela enzima nitrogenase, uma proteína super complexa). Entender e talvez aprimorar essa proteína poderia levar a plantas que fertilizam a si mesmas, uma revolução para a agricultura sustentável.
Parte 5: Limitações e o próximo horizonte
É fácil se empolgar e pensar que o AlphaFold é uma bola de cristal que resolveu a biologia. É uma ferramenta de poder quase inimaginável, mas como toda ferramenta, tem suas limitações. É importante conhecê-las.
- Fotografias em vez de filmes: O AlphaFold prevê uma estrutura 3D estática, uma "foto" da proteína em sua forma mais provável. No entanto, muitas proteínas são dinâmicas. Elas se movem, se contorcem e mudam de forma para funcionar. O próximo grande desafio é prever esse "filme" do movimento das proteínas.
- Interações complexas: O modelo é excelente para prever a estrutura de uma única cadeia de proteína. Ele está melhorando, mas ainda tem dificuldades em prever exatamente como múltiplas proteínas diferentes se encaixam para formar grandes complexos.
- Não cria do zero: O AlphaFold prevê a forma a partir de uma sequência existente. O Santo Graal agora é o problema inverso, o design de proteínas de novo: sonhar com uma função (ex: "quero uma enzima que capture CO2 da atmosfera"), desenhar a forma 3D ideal para essa função e, então, usar IA para descobrir qual sequência de aminoácidos vai se dobrar exatamente naquela forma. O AlphaFold é uma peça-chave nesse processo, mas a jornada está só começando. E uma forma de fazer isso, talvez esteja na Null Tower. Fiz um artigo sobre isso.
Conclusão: Um novo começo
O AlphaFold não é o fim da história. É o fim do começo. Ele não substitui os biólogos, químicos e médicos; ele lhes dá uma superpotência. Ele automatizou uma das etapas mais lentas e frustrantes da pesquisa biológica, liberando as mentes mais brilhantes do planeta para fazerem as perguntas realmente grandes.
Ao resolver o problema do enovelamento de proteínas, a DeepMind não apenas ganhou uma competição. Ela nos deu uma chave-mestra para entender a linguagem da vida. As implicações disso, como vimos, são vastas e vão redefinir o século XXI. Da cura de doenças que assombram a humanidade há gerações à criação de uma economia mais verde e sustentável, estamos à beira de uma era de descobertas que antes pertenciam apenas à imaginação.
Da próxima vez que você ouvir falar de um novo remédio revolucionário ou de uma nova tecnologia para limpar o meio ambiente, lembre-se do AlphaFold. Lembre-se do dia em que uma inteligência artificial nos ajudou a decifrar um dos segredos mais profundos da natureza e, ao fazer isso, nos deu as ferramentas para construir um futuro melhor.

Comments